Autore:
Christy White
Data Della Creazione:
8 Maggio 2021
Data Di Aggiornamento:
1 Luglio 2024

Contenuto
- Al passo
- Metodo 1 di 3: Parte prima: comprensione dei gusci di elettroni
- Metodo 2 di 3: Parte seconda: ricerca di elettroni di valenza nei metalli, eccetto i metalli di transizione
- Metodo 3 di 3: Parte terza: ricerca di elettroni di valenza nei metalli di transizione
- Suggerimenti
- Necessità
Gli elettroni di valenza si trovano nel guscio esterno di un elemento. Il numero di elettroni di valenza in un atomo determina il tipo di legame chimico che questo elemento può formare. Il modo migliore per scoprire il numero di elettroni di valenza è usare la tavola periodica degli elementi.
Al passo
Metodo 1 di 3: Parte prima: comprensione dei gusci di elettroni
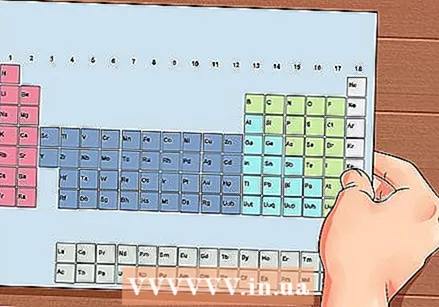 La tavola periodica degli elementi. Questa è una tabella con codici colore, in cui in ogni cella viene visualizzato un elemento con il numero atomico e da 1 a 3 lettere come simbolo.
La tavola periodica degli elementi. Questa è una tabella con codici colore, in cui in ogni cella viene visualizzato un elemento con il numero atomico e da 1 a 3 lettere come simbolo. 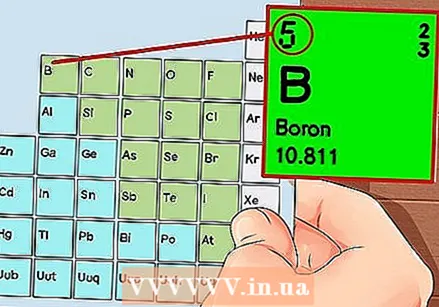 Trova il numero atomico dell'elemento. Il numero atomico è sopra o accanto al simbolo dell'elemento. Ad esempio: il boro (B) ha un numero atomico di 5, il che significa che ha 5 protoni e 5 elettroni.
Trova il numero atomico dell'elemento. Il numero atomico è sopra o accanto al simbolo dell'elemento. Ad esempio: il boro (B) ha un numero atomico di 5, il che significa che ha 5 protoni e 5 elettroni. 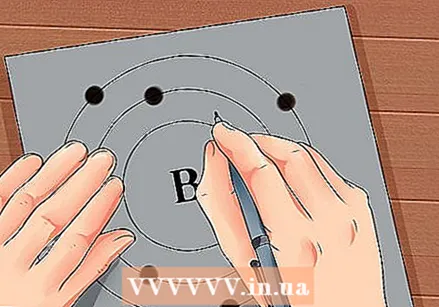 Disegna una semplice rappresentazione di un atomo e posiziona gli elettroni in orbita attorno al nucleo. Questi lavori sono anche chiamati conchiglie o livelli di energia. Il numero massimo di elettroni che possono essere nello stesso guscio è fisso e i gusci vengono riempiti dall'orbita interna a quella esterna.
Disegna una semplice rappresentazione di un atomo e posiziona gli elettroni in orbita attorno al nucleo. Questi lavori sono anche chiamati conchiglie o livelli di energia. Il numero massimo di elettroni che possono essere nello stesso guscio è fisso e i gusci vengono riempiti dall'orbita interna a quella esterna. - K Shell (interno): 2 elettroni massimo.
- L Shell: massimo 8 elettroni.
- M Shell: massimo 18 elettroni.
- N Shell: massimo 32 elettroni.
- O Shell: massimo 50 elettroni.
- P Shell (esterno): 72 elettroni massimo.
 Trova il numero di elettroni nel guscio esterno. Questi sono gli elettroni di valenza.
Trova il numero di elettroni nel guscio esterno. Questi sono gli elettroni di valenza. - Quando il guscio di valenza è pieno, l'elemento è stabile.
- Se il guscio di valenza non è pieno, l'elemento è reattivo, il che significa che può legarsi chimicamente con l'atomo di un altro elemento. Ogni atomo condivide i suoi elettroni di valenza nel tentativo di riempire il guscio di valenza.
Metodo 2 di 3: Parte seconda: ricerca di elettroni di valenza nei metalli, eccetto i metalli di transizione
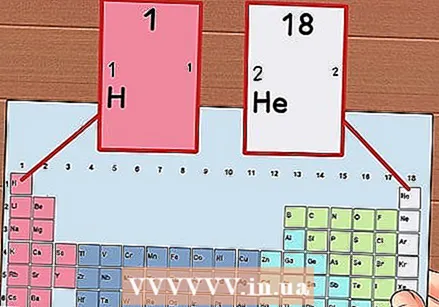 Numerare ogni colonna della tavola periodica, da 1 a 18. L'idrogeno (H) è in cima alla colonna 1 e l'elio (He) in cima alla colonna 18. Questi sono i diversi gruppi di elementi.
Numerare ogni colonna della tavola periodica, da 1 a 18. L'idrogeno (H) è in cima alla colonna 1 e l'elio (He) in cima alla colonna 18. Questi sono i diversi gruppi di elementi. 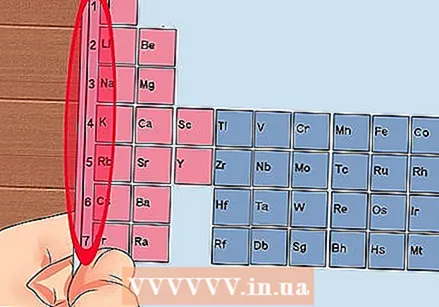 Assegna un numero a ciascuna riga, da 1 a 7. Questi sono i periodi degli elementi e corrispondono al numero di gusci o livelli di energia di un atomo.
Assegna un numero a ciascuna riga, da 1 a 7. Questi sono i periodi degli elementi e corrispondono al numero di gusci o livelli di energia di un atomo. - Idrogeno (H) ed Elio (He) hanno entrambi 1 guscio, mentre Francium (Fr) ne ha 7.
- I lantanidi e gli attinidi sono raggruppati ed elencati sotto la tabella principale. Tutti i lantanidi appartengono al Periodo 6, Gruppo 3 e tutti gli attinidi appartengono al Periodo 7, Gruppo 3.
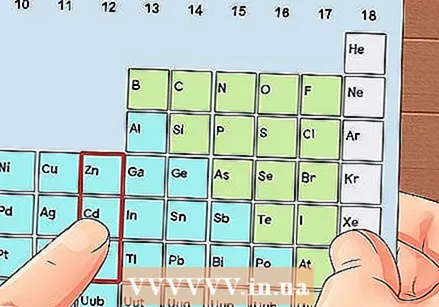 Individua un elemento che non sia un metallo di transizione. I metalli di transizione sono nei gruppi da 3 a 12. I numeri di gruppo degli altri metalli indicano il numero di elettroni di valenza.
Individua un elemento che non sia un metallo di transizione. I metalli di transizione sono nei gruppi da 3 a 12. I numeri di gruppo degli altri metalli indicano il numero di elettroni di valenza. - Gruppo 1: 1 elettrone di valenza
- Gruppo 2: 2 elettroni di valenza
- Gruppo 13: 3 elettroni di valenza
- Gruppo 14: 4 elettroni di valenza
- Gruppo 15: 5 elettroni di valenza
- Gruppo 16: 6 elettroni di valenza
- Gruppo 17: 7 elettroni di valenza
- Gruppo 18: 8 elettroni di valenza - tranne l'elio, che ne ha 2
Metodo 3 di 3: Parte terza: ricerca di elettroni di valenza nei metalli di transizione
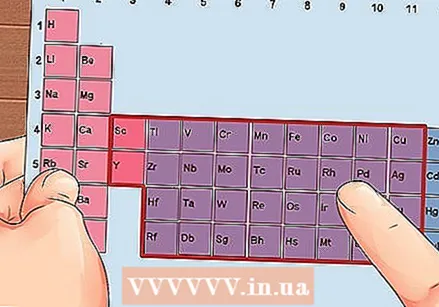 Trova un elemento dai gruppi 3 a 12, i metalli di transizione.
Trova un elemento dai gruppi 3 a 12, i metalli di transizione. Determina il numero di elettroni di valenza in base al numero del gruppo. Questi numeri di gruppo corrispondono a un numero possibile di elettroni di valenza.
Determina il numero di elettroni di valenza in base al numero del gruppo. Questi numeri di gruppo corrispondono a un numero possibile di elettroni di valenza. - Gruppo 3: 3 elettroni di valenza
- Gruppo 4: da 2 a 4 elettroni di valenza
- Gruppo 5: da 2 a 5 elettroni di valenza
- Gruppo 6: da 2 a 6 elettroni di valenza
- Gruppo 7: da 2 a 7 elettroni di valenza
- Gruppo 8: 2 o 3 elettroni di valenza
- Gruppo 9: 2 o 3 elettroni di valenza
- Gruppo 10: 2 o 3 elettroni di valenza
- Gruppo 11: 1 o 2 elettroni di valenza
- Gruppo 12: 2 elettroni di valenza
Suggerimenti
- I metalli di transizione possono avere gusci di valenza che non sono completamente pieni. Determinare il numero esatto di elettroni di valenza nei metalli di transizione richiede alcuni principi della teoria quantistica che esulano dallo scopo di questo articolo.
Necessità
- Tavola periodica degli elementi
- Matita
- Carta