Autore:
Louise Ward
Data Della Creazione:
11 Febbraio 2021
Data Di Aggiornamento:
1 Luglio 2024

Contenuto
La dimensione di un atomo è così piccola che è difficile misurare con precisione il numero atomico di un composto chimico. Per essere in grado di misurare con precisione una quantità di sostanze, gli scienziati utilizzano un'unità di mole per rappresentare un numero specificato di atomi. Una mole di sostanza è definita come equivalente al numero di atomi di carbonio contenuti in 12 grammi di isotopo di carbonio, che è di circa 6.022 x 10 atomi. Questo valore è chiamato numero di Avogadro o costante di Avogadro. Questo è anche indicato come il numero di atomi in 1 mole di qualsiasi elemento e 1 mol della massa di una sostanza è chiamata massa molare di quella sostanza.
Passi
Metodo 1 di 2: calcola la massa molare di un elemento
Definizione molar mass. La massa molare di una sostanza è la massa (in grammi) di una mole di quella sostanza. Per calcolare la massa molare di un elemento, moltiplica la sua massa atomica per il fattore di conversione grammi per mole (g / mol).
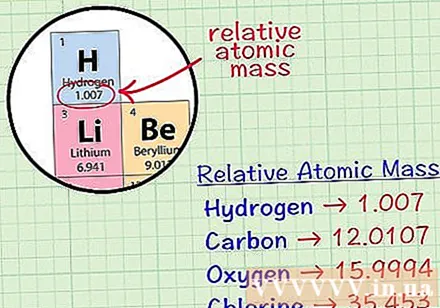
Trova l'atomo cubico medio di un elemento. L'atomo di massa media di un elemento è la massa media, in unità atomiche, in un campione che include tutti gli isotopi di quell'elemento. Queste informazioni sono spesso fornite nella tavola periodica degli elementi. Individuando un elemento, puoi trovare un atomo cubico medio scritto appena sotto il simbolo chimico dell'elemento. Questo valore non è un numero intero, ma un numero con decimali.- Ad esempio, con l'idrogeno, l'atomo di massa media è 1,007; L'atomo cubico medio di carbonio è 12,0107; L'atomo di massa media di ossigeno è 15.9994; il cloro ha una massa atomica media di 35.453.

Moltiplica l'atomo di massa media per la costante di massa molare. L'unità di scorrimento molare è definita come 0,001 chilogrammo per mol o 1 grammo per mol. Il prodotto dell'atomo di massa media e della costante di massa molare converte l'unità di massa atomica in grammi per mole, quindi la massa molare dell'idrogeno sarà 1.007 grammi per mole, del carbonio è 12. , 0107 grammi per mole, di ossigeno è 15,9995 grammi per mole e quello del cloro è 35,453 grammi per mole.- Alcuni elementi esistono in natura come molecole costituite da due o più degli stessi atomi. Cioè, se vuoi calcolare la massa molare di composti costituiti da più di un atomo, come gas idrogeno, gas ossigeno o gas cloro, devi determinare la massa atomica media del composto e moltiplicare questo valore. con la costante di massa molare, '' poi '' moltiplica il prodotto che hai appena trovato per 2.
- Con H2: 1.007 x 2 = 2.014 grammi per mol; per O2: 15.9994 x 2 = 31.9988 grammi per mol; e Cl2: 35.453 x 2 = 70.096 grammi per mol.
Metodo 2 di 2: calcola la massa molare del composto

Determina la formula strutturale del composto. La formula strutturale di una sostanza fornisce il numero atomico di ogni elemento che compone quel composto. (Queste informazioni sono disponibili in tutti i libri di riferimento). Ad esempio, la formula chimica dell'acido cloridrico è HCl; di glucosio è C6H12O6. Con questa formula strutturale, possiamo determinare il numero di ciascun tipo di atomo che costituisce il composto in esame.- Dove HCl ha un atomo di idrogeno e un atomo di cloro.
- Molecola di zucchero glucosio C6H12O6 ha 6 atomi di carbonio, 12 atomi di idrogeno e 6 atomi di ossigeno.
Determina l'atomo di massa media di ciascun elemento costituente. Usa la tavola periodica per trovare l'atomo di massa media di ogni elemento presente nel composto. L'atomo di massa media è solitamente scritto sotto il simbolo chimico dell'elemento sulla tavola periodica. Simile al calcolo della massa molare di un elemento, moltiplica l'atomo di massa media per 1 grammo / mol.
- L'atomo di massa media degli elementi che formano acido cloridrico è il seguente: idrogeno 1.007 g / mol e cloro 35.453 g / mol.
- L'atomo di massa media degli elementi che compongono la molecola di glucosio è: carbonio, 12.017 g / mol; idrogeno, 1.007 g / mol; e ossigeno, 15,9995 g / mol.
Calcola la massa molare di ogni elemento componente. Moltiplicando l'atomo di massa di un elemento per il numero di atomi a cui contribuisce in un composto si ottiene la massa media dell'elemento nel composto.
- Nel caso dell'acido cloridrico, acido cloridrico, la massa molare dell'elemento idrogeno è 1.007 g / mol e quella del cloro è 35.453 g / mol.
- Nel caso del glucosio, C6H12O6, la massa molare di ciascun elemento è la seguente: carbonio, 12,0107 x 6 = 72,0642 g / mol; idrogeno, 1.007 x 12 = 12.084 g / mol; ossigeno, 15.9995 x 6 = 95.9964 g / mol.
Massa molare totale degli elementi costitutivi. La massa molare totale degli elementi di compostaggio è la massa molare del composto.Nel passaggio precedente abbiamo calcolato la massa molare di ogni elemento presente nel composto, in questo passaggio dobbiamo solo sommare tutti questi valori insieme.
- La massa molare dell'acido cloridrico è 1.007 + 35.453 = 36.460 g / mol. 36,46 grammi è la massa di 1 mol di acido cloridrico.
- La massa molare del glucosio è 72,0642 + 12,084 + 95,9964 = 180,1446 g / mol. Quindi ogni mole di glucosio ha una massa di 180,14 grammi.
Consigli
- Sebbene nella maggior parte dei casi, l'atomo di massa media sia registrato con l'approssimazione di 1 parte 1000 (4 cifre decimali), nei laboratori la massa molare è spesso ridotta a 2 cifre decimali, a volte anche meno, per le grandi molecole. Pertanto, nel caso di laboratorio, la massa molare dell'acido cloridrico può essere scritta come 36,46 grammi per mol, per il glucosio 180,14 grammi per mol.
Quello di cui hai bisogno
- Libro di riferimento chimico o tavola periodica degli elementi
- Computer